前有魏则西、后有张煜医生举报,细胞免疫疗法五年遭遇三重罗生门
在癌症患者遭遇人财两空的悲剧中,“治疗方法”往往是众矢之的。
5年前,魏则西接受细胞免疫治疗(DC-DIK疗法,树突状细胞和细胞因子活化杀伤细胞联合回输),救治无果去世;今年4月,“北医三院肿瘤内科医生反映肿瘤治疗黑幕”事件中,患者马进仓接受的NK疗法也遭到质疑。
引发公共舆论事件的这两起医疗纠纷,有着耐人寻味的相似之处——惹祸的DC-DIK和NK,都属于“细胞免疫疗法”。某种程度上,正是它们让魏则西和马进仓踏入了同一条河流。
细胞免疫疗法,全称“被动性细胞免疫治疗”。方法是:从血液或肿瘤中分离出免疫细胞,体外培养(或通过基因工程改造,使免疫细胞表达肿瘤特异性受体),再输回患者体内,以期实现缓解乃至治愈的目的[1]。目前,有多种免疫细胞可供使用,如自然杀伤细胞(NK细胞)、淋巴因子活化杀伤细胞(LAK细胞)、细胞毒性T细胞(CTL细胞)、树突状细胞(DC细胞)等。
但并非所有细胞免疫疗法都不靠谱。以CAR-T为例,就已有产品获FDA批准上市,且这类疗法大概率会在今年内落地中国。
如果没有魏则西事件,CAR-T进入中国的步伐也许会更快一些……
艾马殊 | 作者
一萌、普通酱 | 编辑
放大灯团队 |策划

生命的奇迹,都已明码标价
2010年5月,年仅5岁的小女孩艾米莉·怀特黑德(Emily Whitehead)被诊断出患有急性淋巴细胞白血病。2012年4月,艾米莉前往美国费城儿童医院(CHO),成为了首个接受CAR-T疗法的儿童患者。
经过治疗,艾米莉恢复了健康,并生活至今[2]。需要指出的是,CAR-T疗法并非一劳永逸,艾米莉也在接受CHO长期的随访和监测。
CAR-T,即嵌合抗原受体T细胞免疫疗法(Chimeric Antigen Receptor T-Cell Immunotherapy)——通过采集患者外周血并提取T细胞,将T细胞在体外进行改造,令其识别肿瘤细胞表面的抗原。然后把这些细胞回输给病人,进而识别并杀死肿瘤细胞。

CAR-T治疗过程示意图 来源 | 药明巨诺招股书
围绕CAR-T,全球范围内的科研机构和创新药企展开了大量研究和合作。在国外,诺华(Novartis)、凯特制药(Kite Pharma)、朱诺医疗(Juno Therapeutics)等企业的研发进度比较领先。
在研发竞赛中夺得头筹的是诺华—2017年8月,诺华的CAR-T疗法Kymriah获批上市,用于治疗25岁以下患者的B细胞急性淋巴细胞白血病(ALL)。
Kymriah的治疗效果几何?
经独立中心审查评估的数据显示,在63例可评价疗效的患者中,Kymriah的疗法总体缓解率为82.5%,包括63%的完全缓解患者和19%的完全缓解但血液系统不完全恢复患者[3]。
奇迹不会平白发生。生存的希望,也被标上了昂贵的价格。
Kymriah需要量身定做,且治疗流程复杂,定价高达47.5万美元;比它晚一个半月上市的另一款CAR-T疗法——凯特制药的Yescarta,定价也高达37.3万美元。
在CAR-T研发竞赛中,中国企业跑得并不慢。
为了将CAR-T引进中国,早在2016年2月,药明康德和朱诺就成立了合资公司药明巨诺;2017年4月,复星医药也与凯特制药合资成立公司复星凯特。
但对中国的企业们来说,CAR-T落地还需漫长的等待。这与魏则西事件,又有密不可分的关系。

一放就乱
DC-CIK疗法在国外早已淘汰,但它能堂而皇之地用在魏则西身上,一部分原因,要归咎于当时混乱无序的行业。

中国医药教育协会制药技术专业委员会常务委员刘双生就曾表示,三类医疗技术的应用需要备案,但当时根本没有有效的监管。“就是报一个备案,几个人过来看一下。达不达到标准,他也没有水平(判断)。到后期实施时,也没有飞行检查的约束。”当时,建几个小实验室,就可以开始开展三类医疗技术的应用[4]。
在2009年到2015年这个时期,很多小型医院不经过行政部门准入审批,就在开展细胞免疫治疗。细胞免疫治疗成了当时一些民营医疗企业的“摇钱树”和虚假医疗广告的重灾区。
澎湃新闻的调查发现,细胞免疫治疗多采取“前店后厂”模式——免疫细胞治疗企业与医院合作,企业负责细胞培养工作,前期诊断、抽血,后期回输等工作则由医院完成。魏则西就诊的北京武警二院肿瘤生物中心,就是由莆田系实际控制的康新公司以承包入股方式,与院方展开合作[5]。
细胞免疫疗法是不是应按药品进行监管?卫生部门内部意见不一。但在实际操作中,细胞免疫疗法一直按照“第三类医疗技术”进行管理。
这意味着,与“药品”(转由食药监局进行管理)相比,细胞免疫治疗规范流程如何进行、细胞如何制备、治疗风险如何控制等行业标准一直未能建立。

一管就死
魏则西去世后,监管部门迅速对细胞免疫治疗行业开展整顿。
2016年5月4日,当时的国家卫生计生委召开会议,提出了一系列监管要求。这些要求包括禁止医疗机构出租科室、发布虚假医疗广告等。同时明确,自体细胞免疫治疗技术仅限于临床研究。

2016年5月4日,国家卫生计生委召开规范医疗机构科室管理和医疗技术管理工作电视电话会议
野蛮生长了多年的细胞免疫治疗行业,被紧急按下暂停键。
以深圳为例,卫计委紧急规范一年后,深圳80%的细胞免疫相关企业关门。剩下的20%进行了至少一半的裁员,技术人员约九成流失到其它行业[5]。
一方面,细胞免疫行业受到重创;另一方面,公众也因此对免疫疗法持负面态度。对于细胞免疫疗法,人们多少有了些“谋财害命”的印象。而在一些专家看来,就此否定所有细胞免疫疗法,并不可取。
2017年,时任清华大学医学院院长、免疫学研究所所长董晨就在一场采访中表示,把DC-CIK疗法等同于免疫疗法并不准确,否定所有免疫疗法是一叶障目[6]。在这场采访里,董晨也提到了CAR-T:“现在这个技术方兴未艾,在白血病治疗中有显著疗效。”

他们治愈了癌症,我们呢?
在中国,由于魏则西事件的影响,国内细胞免疫治疗行业遭遇“政策冷冻”。
直到2017年10月23日,“解冻”开始。原食品药品监管总局就《药品注册管理办法》修订稿征求意见,拟将细胞治疗产品列入药品进行审批[7]。接下来的两个月里,《治疗用生物制品注册受理审查指南(试行)》和《细胞治疗产品研究与评价技术指导原则》陆续发布。细胞免疫治疗管理基本实现了由“医疗技术”向“药品”的过渡。
政策步入正轨,影响立竿见影。
这一年的12月11日,传奇生物提交的 CAR-T(CXSL1700201)临床申请获得 CDE承办受理,成为首个获受理的国产CAR-T。自此,国内公司开始了CAR-T疗法临床试验的竞赛。
2017年以后,细胞免疫治疗领域的管理、审查政策及技术标准逐渐出台。

到了2021年1月12日,复星凯特的CAR-T疗法益基利仑赛注射液在中国的上市申请变更为“在审批”。虽然2月18日这一状态又变更为“排队待审评”,需补充临床及药学资料,但业内普遍认为,中国首款CAR-T疗法上市已近在眼前。
而此时(2021年2月),全球已经有四款CAR-T疗法获FDA批准上市了。

注:2021年了3月26日,FDA又批准了CAR-T疗法Abecma上市。目前,全球共五款CAR-T上市。

千亿中国市场
CAR-T一旦在中国落地,对于患者来说,最关心的莫过于价格。
就国外几款疗法而言,患者负担在37.5万~47.5万美元。高昂的价格并没有阻止这些孤儿药的市场增长。根据诺华和吉利德的财报,短短几年间,CAR-T产品的年销售额已超10亿美元。
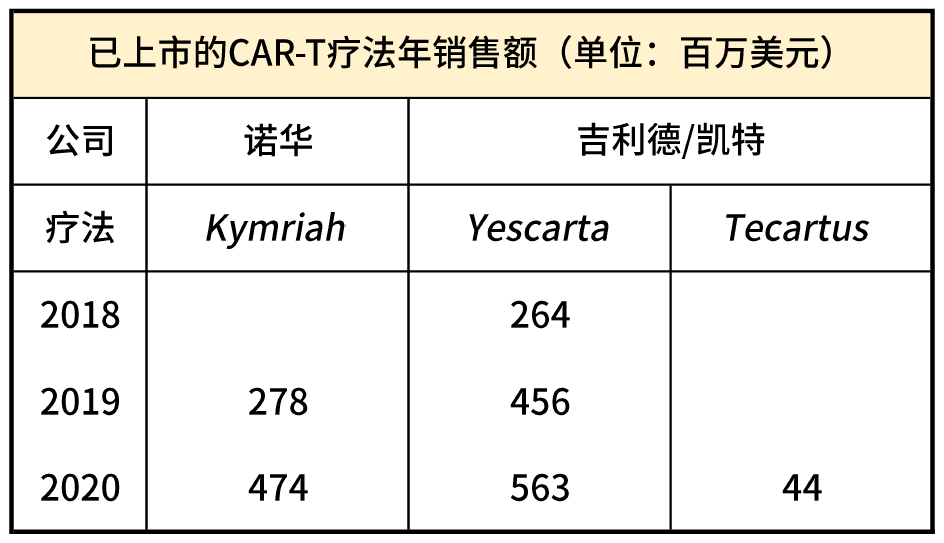
三款CAR-T疗法年销售额。放大灯团队丨整理
有观点认为,CAR-T进入中国,定价会低于美国市场,但治疗费用仍将高达百万人民币左右[8]。高昂的治疗费会熄灭大家对于CAR-T疗法的热情吗?
也不一定。
咨询机构Frost Sullivan测算,随着CAR-T在中国审批上市,到2026年,中国CAR-T市场的规模就可达到107亿。从2021~2030这十年间,整个市场累计规模可达千亿之巨。
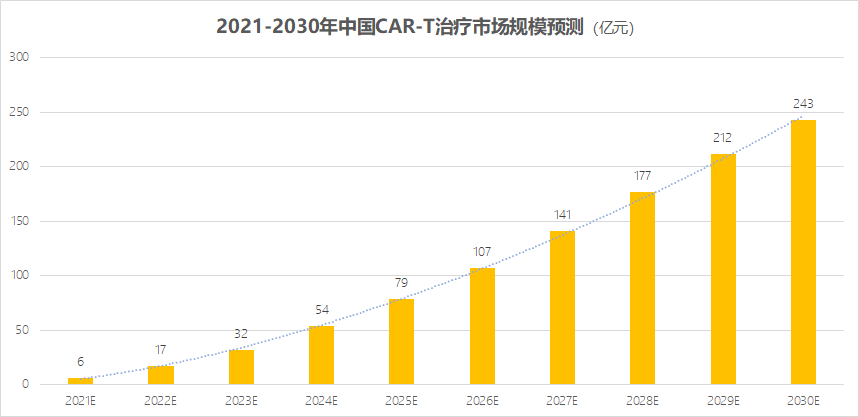
数据来源:Frost Sullivan 放大灯团队制图
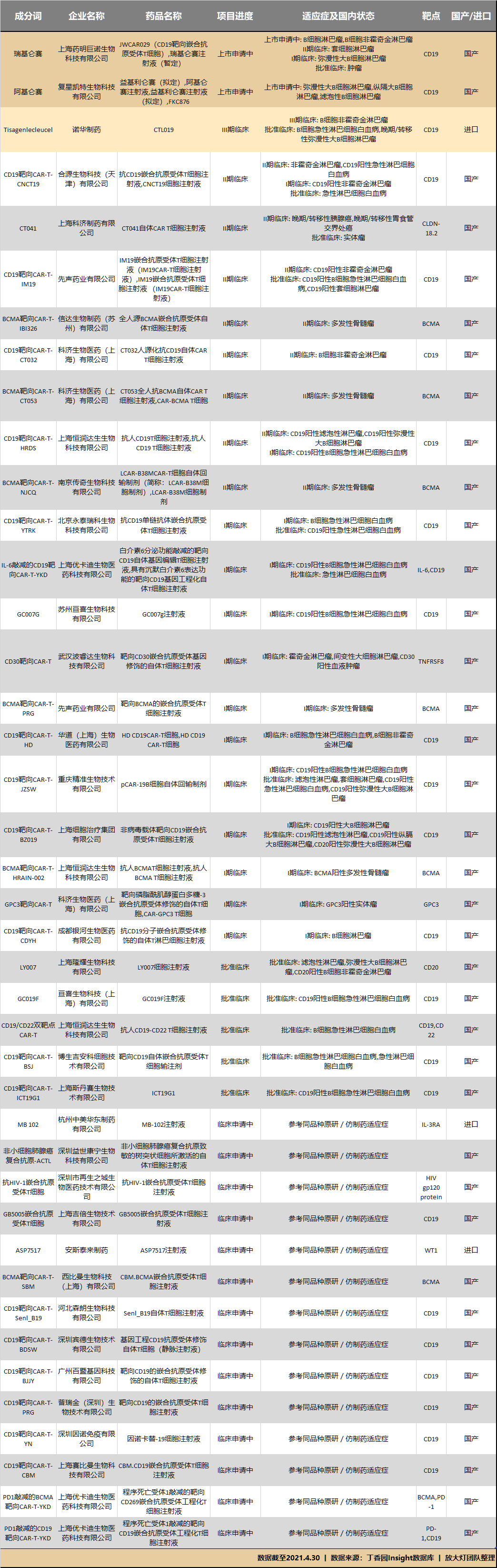
广阔的市场自然也吸引到众多企业入局。丁香园Insight的数据显示,国内申请及进入临床试验阶段的CAR-T疗法,已有40余个。
(上下滑动查看,数据截至2021年4月30日)
这是每个创新药物都要走的路:海外过审、面对热门疗法的跟风研发、在中国市场的艰难审批……CAR-T从FDA审批到中国有望上市,用时近四年。这也许是创新药行业可以接受的速度,但对很多患者来说,却成了永远的遗憾。
用得好,免疫疗法是救命天使;但医生用得不对症、监管混乱反而会让它成为魔鬼。这是细胞免疫疗法五年来遭遇的三重罗生门。

References: