Nature:清华陈柱成团队解析人源PBAF染色质重塑复合物结合核小体的结构
2022年4月27日,清华大学生命科学学院/结构生物学高精尖创新中心/清华-北大生命科学联合中心陈柱成教授研究团队在《自然》在线发表题为“人源PBAF染色质重塑复合物结合核小体的结构”(Structure of human PBAF chromatin remodeling complex bound to a nucleosome)的研究论文。该论文报道了人源染色质重塑复合物PBAF在活性状态下结合核小体的结构,揭示了由12个亚基组成的PBAF复合物的组装方式,识别核小体的机制,为众多与人类疾病相关突变的致病机理提供了理论框架。

网页截图
在真核生物中,DNA缠绕在组蛋白上形成核小体,经高度压缩形成染色质。这一形式一方面保证了基因组的稳定性,另一方面阻碍了诸如遗传信息的复制,转录和DNA损伤修复等生命活动。因此,染色质的动态调控对于生物具有重要作用。染色质重塑Snf2-家族马达蛋白利用ATP的能量来滑动、弹出、交换或解聚核小体,从而实现对染色质的动态调控。
BAF(BRG1-associated factors)和PBAF(polybromo-associated BRG1-associated factors)是哺乳动物SWI/SNF家族的染色质重塑复合物, 它们调控染色质结构和基因表达,广泛参与动物细胞的发育分化过程。近年来,随着高通量测序技术的发展,科研人员发现BAF/PBAF复合物的突变与超过20%的癌症及多种神经系统发育缺陷有关,该复合物也可视为治疗癌症等重大疾病的潜在药物靶点。
科学界因此广泛关注SWI/SNF家族复合物,尽管早在1996年BAF/PBAF复合物就已得到鉴定,但其组装方式和染色质重塑机制一直尚不明确。得益于冷冻电镜技术的发展,酵母SWI/SNF家族复合物及人源BAF复合物的高分辨结构先后在2019和2020年得以报道,然而PBAF复合物的组装方式、识别核小体的机制及其与BAF复合物的差异等问题还尚待研究。尤其是已报道的BAF复合物核心马达亚基(SMARCA4/BRG1)处于非活性状态,不能明确许多与疾病相关突变的致病机理。
陈柱成教授研究团队长期深耕于染色质重塑领域,并带领团队基于此前一系列重要成果不断突破,克服技术难点,通过体外重组的方法获得了高质量的PBAF复合物,利用冷冻电子显微镜技术,解析了PBAF结合核小体的高分辨结构(3.4埃)。
PBAF复合物的12个亚基根据功能不同,可以分成3个模块:发挥催化活性的motor模块,具有调控功能的ARP (actin-related protein)模块,和发挥染色质靶向功能的SRM模块(substrate recruitment module)。其中,PBAF的9个辅助亚基穿梭交织在一起,形成一个三叶片状的SRM模块。这些叶片根据其主要生物学功能,被命名为:核小体结合叶片(nucleosome-binding lobe,NBL),组蛋白尾巴结合叶片(histone-tail-binding lobe, HBL)和DNA结合叶片(DNA-binding lobe,DBL)。与BAF相比,HBL是PBAF特有的模块,包含特异亚基PBRM1、PHF10和BRD7。这些亚基拥有11个结合组蛋白尾巴的结构域。研究人员认为,这相当于一个超级组蛋白识别亚模块,有利于PBAF复合物在机体中更高效地感知染色质信号,发挥染色质重塑功能。这项工作提出了PBAF结合转录因子(TF)来调控基因表达的可能机理,同时也揭示了ARID2、PBRM1等亚基位点突变致病的可能机理。
值得注意的是本研究解析的复合物中马达亚基SMARCA4处于活性状态,在此结构中我们可以清楚地看到,疾病相关的突变主要位于高度保守的ATP结合口袋周围,以及新形成的Brace-helix界面。Brace-helix活性界面介导了两个马达结构域(Lobe1与Lobe2)的相互作用,是耦合ATP水解和核小体滑动的关键元件,该结构由陈柱成研究组于2017年首次在酵母染色质重塑蛋白Snf2发现。
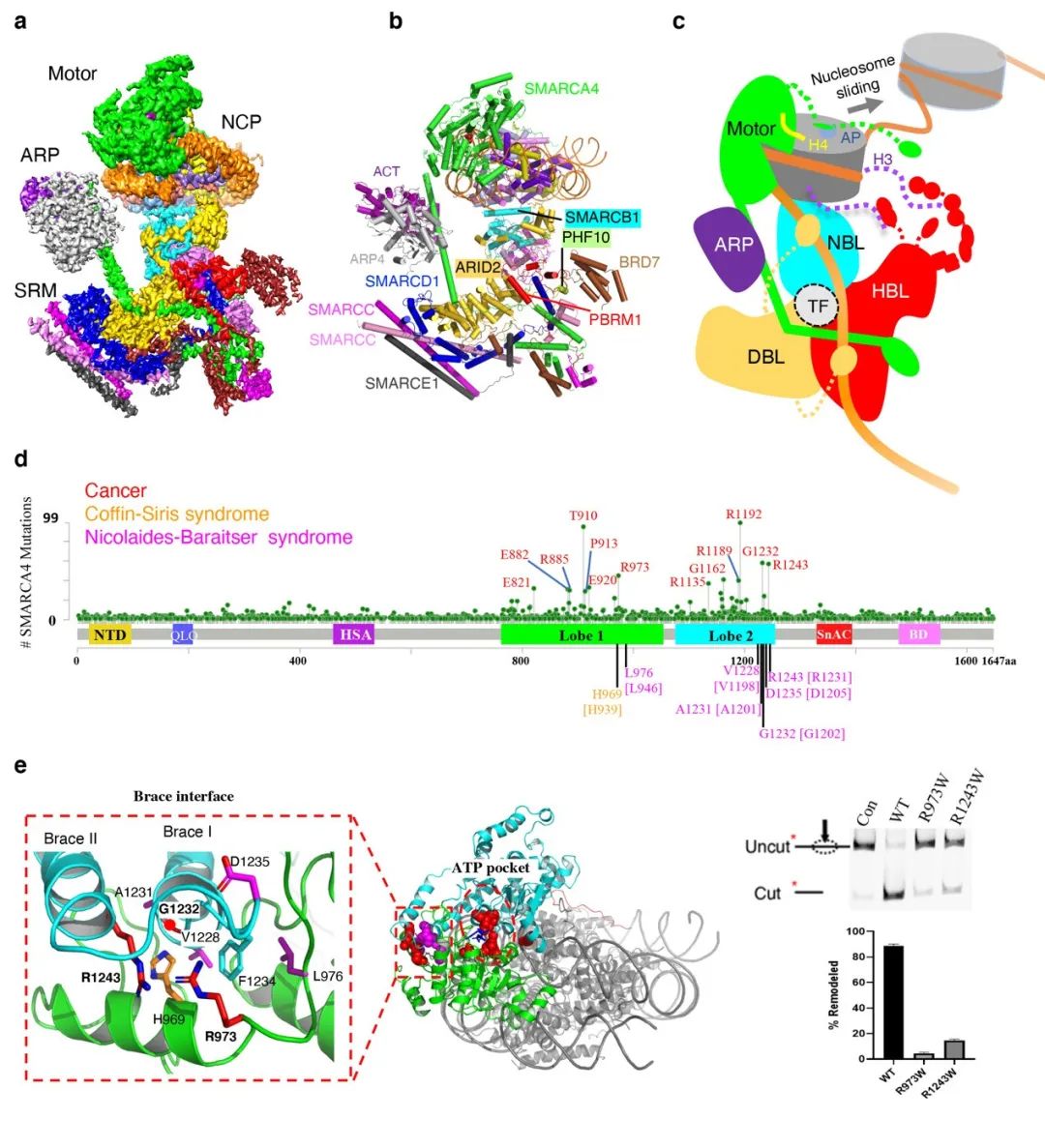
PBAF染色质重塑复合物结合核小体的结构和疾病相关突变
(a)PBAF-核小体复合物的冷冻电镜密度图。(b)PBAF-核小体复合物的结构模型。(c)PBAF复合物识别核小体,调控染色质结构的模型。(d)癌症及神经系统发育缺陷综合征相关相关的SMARCA4/2的错义突变位点分布(数据来自COSMIC,cBioPortal和已发表文献)。SMARCA4序列为参考,标记高频突变位点;SMARCA2突变的对应氨基酸残基在[]里。(e)疾病相关的突变位点主要位于“ATP pocket”周围和“Brace interface”,局部放大图显示了高频突变位点在Brace-helix界面的分布,右图生化实验显示R973和R1243的突变大大降低了染色质重塑活性 | 团队供图
在PABF的研究工作中,他们还发现在新形成的Brace-helix界面上存在多个与癌症相关的SMARCA4高频突变热点,及多个发生在旁系同源蛋白SMARCA2上与神经系统发育缺陷相关的突变。生化实验证实了这些位点的突变会显著降低染色质重塑活性,这提示含有这些突变变位点的病人的BAF/PBAF复合物功能的丧失。另外,高质量的电镜密度首次揭示了SMARCA4亚基的SnAc 结构域识别核小体的机制:SnAc通过3个“arginine anchor”识别核小体的酸性口袋,促进染色质重塑活性。
总之,这项工作不仅阐明了PBAF复合物组装、核小体识别和染色质重塑机制,也为理解BAF/PBAF突变相关的致病机理提供了理论基础,这一发现有利于在染色质水平理解染色质重塑机制,也会推动相关疾病靶向药物的研发。
参考文献
Yuan, J., Chen, K., Zhang, W. et al. Structure of human chromatin-remodelling PBAF complex bound to a nucleosome. Nature (2022). https://doi.org/10.1038/s41586-022-04658-5
作者:陈柱成实验室
编辑:酥鱼
排版:尹宁流
题图来源:团队供图
研究团队
通讯作者 陈柱成:清华大学生命科学学院/结构生物学高精尖创新中心/清华-北大生命科学联合中心教授
(共同)第一作者 袁俊杰:清华大学生命科学学院/清华-北大生命科学联合中心2019级博士生
(共同)第一作者 陈康净:清华大学生命科学学院2017级博士生
博士后张文博也参与了重要工作。
本工作获得国家自然科学基金、科技部重大科学研究计划专项、北京市结构生物学高精尖创新中心、清华-北大生命科学联合中心、国家蛋白质科学研究(北京)设施清华基地的大力支持。
论文信息
发布期刊 《自然》 Nature
发布时间 2022年4月27日
论文标题 Structure of human chromatin-remodelling PBAF complex bound to a nucleosome
(DOI:https://doi.org/10.1038/s41586-022-04658-5)
未来光锥加速器是果壳硬科技发起的早期科技创业加速器,为科学家创业提供从公司注册、知识产权,到融资需求、团队组建等不同阶段的方案建议。加速科技成果从实验室到市场的转化,加速一部分科学家迭代成为CEO。
果壳团队有着长达12年为科学家服务的经验,我们始终站在科学家的视角出谋划策,做科创者的好朋友。如果您正打算创办一家科技企业,无论是找钱、找人、找资源,还是找订单,都欢迎与未来光锥团队聊聊。您可发送bp或其他项目资料到wlgz@guokr.com,并留下联系方式,或添加果壳硬科技企业微信,私信沟通。

✦
✦
点击阅读原文即可查看原论文

